Jak zapisać się na kurs nurkowania!
Kursy nurkowania prowadzimy w Krakowie. Zależy ci na szybkim terminie - skontaktuj się z instruktorem
Tel.: (+48) 501 627 846. lub e-mail. Zawsze możesz zadzwonić i zapytać. Preferujemy kontakt telefoniczny. Więcej.
Prawo Daltona (prawo ciśnień parcjalnych)
fizyka nurkowania
Umiejętność wyliczania ciśnienia parcjalnego danego gazu jest niezwykle ważna, bo to ciśnienie parcjalne decyduje o oddziaływaniu danego gazu na naszą fizjologię czyli zachowaniu się naszego organizmu pod wodą. Tematy związane z ciśnieniem parcjalnym powinny być znane wszystkim płetwonurkom a w szczególności nurką którzy stosują mieszanki oddechowe inne niż powietrze (nitrox, trimix),
Prawo ciśnień parcjalnych
Ciśnienie mieszaniny gazów równa się sumie ciśnień, jakie wywierałyby poszczególne składniki gazu gdyby były same w danej objętości (ciśnienie jakie wywierałby gaz gdyby znajdował się sam w zbiorniku).
Ciśnienie całkowite mieszaniny gazowej jest równe sumie ciśnień parcjalnych wszystkich składników.
Ptot = PP1 + PP2 + ... + PPn [at] (1)
gdzie:
Ptot - ciśnienie całkowite (absolutne) mieszaniny gazów
PP1 - ciśnienie parcjalne gazu 1 (Partial preasure)
PP2 - ciśnienie parcjalne gazu 2
PPn - ciśnienie parcjalne gazu n-tego
Każdemu składnikowi mieszaniny możemy przypisać tzw. ciśnienie parcjalne PP, będące iloczynem ciśnienia całkowitego Ptot i jego procentowej zawartości objętościowej czyli frakcji F (wyrażonej w setnych częściach z całości).
PP = Ptot * F [at] (2)
Przykładowo procentowa zawartość (frakcja) tlenu O2 w powietrzu atmosferycznym (czyli dla ciśnienia 1at) wynosi 21%, po zamianie na setne będzie to F=0,21 czyli otrzymamy:
PPO2 = 1at * 0,21 = 0,21at
Dla azotu N2 znajdującego się w powietrzu atmosferycznym (79%) będzie to:
PPN2 = 1at * 0,79 = 0,79at
Jeżeli chcemy obliczyć ciśnienie parcjalne danego gazu na dowolnej głębokości we wzorze (2) musimy uwzględnić zwiększenie ciśnienia całkowitego (absolutnego). Ciśnienie całkowite jest równe ciśnieniu atmosferycznemu i hydrostatycznemu i można je obliczyć z wzoru:
Ptot = D/10 + 1 [at] (3)
gdzie: D - głębokość wyrażona w metrach [m]
połączenie wzoru (2) i (3) da nam:
PtotPP = (D/10 + 1) * F [at]
Przykładowo ciśnienie parcjalne na głębokości 30m dla tlenu o frakcji FO2=0,21 wyniesie
PPO2 = (30/10+1) * 0,21 = 4 * 0,21 = 0,84at
jeżeli jednak nurkowanie będzie na nitroksie o frakcji tlenu FO2=0,36 to otrzymamy ciśnienie parcjalne tleny:
PPO2 = (30/10+1) * 0,36 = 4 * 0,36 = 1,44at
W nurkowaniu amatorskim w trakcie zanurzania nie wolno przekraczać ciśnienia parcjalnego tlenu 1,4at stąd wniosek, że nie jest to już właściwa mieszanka dla tej głębokości.
Oczywiście możemy mieć również przypadek odwrotny w czasie nurkowania na trimiksie w którym frakcja tlenu FO2=0,04, po wstawieniu wartości do wzoru otrzymamy:
PPO2 = (30/10+1) * 0,04 = 4 * 0,04 = 0,16at
Taką mieszanką nie da się oddychać i albo należy zmienić skład mieszanki albo głębokość na której zakończymy na tej mieszance oddychać.
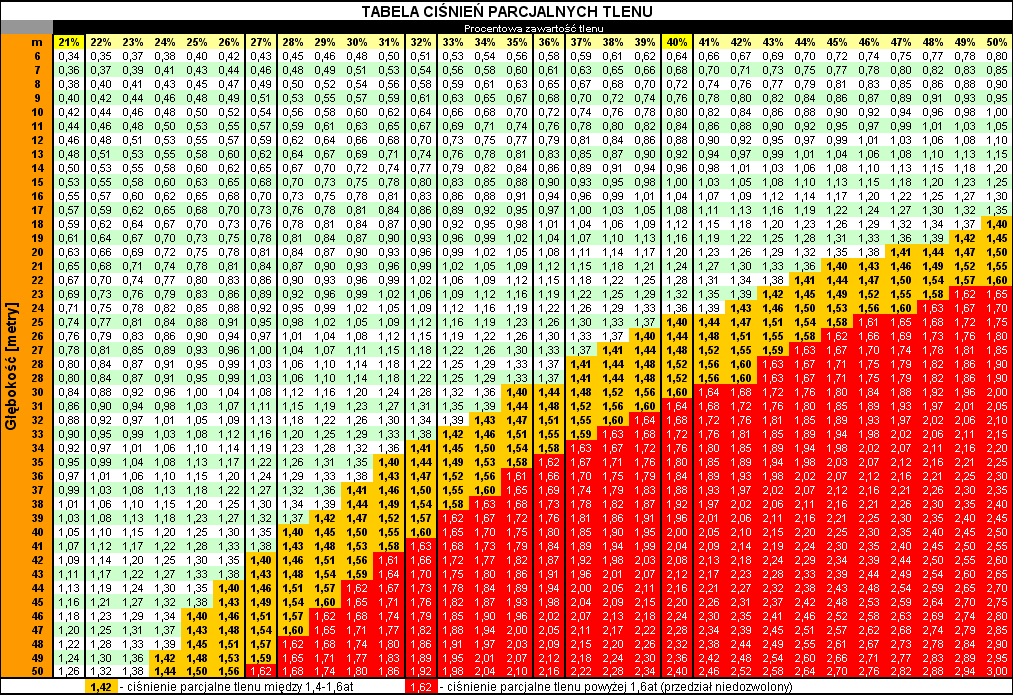
Są również, odpowiednie tabele, np. tabela ciśnień parcjalnych tlenu. Stosowanie tabel jest wygodne, zwalnia nas z obliczeń, dzięki czemu redukuje ilość pomyłek.
Zadania
W identyczny sposób można policzyć ciśnienia parcjalne dla pozostałych gazów: azotu i helu.
Korzystając z powyższego wzoru możemy obliczyć:
Zadanie 1
Oblicz ciśnienie parcjalne azotu i tlenu w powietrzu atmosferycznym?
Korzystamy z prawa Daltona (ciśnień parcjalnych)
Pazotu=78%*P0=0,78*1at=0,78at,
Ptlenu=21%*P0=0.21*1at=0.21at
Zadanie 2
Do jakiej głębokości można nurkować na powietrzu przy założeniu, że dopuszczalne ciśnienie parcjalne tlenu przy którym tlen nie jest toksyczny wynosi 1.6at.?
Należy ułożyć proporcję która odpowie na pytanie przy jakiej głębokości zostanie przekroczone ciśnienie parcjalne 1,6at. Na powierzchni (1at) ciśnienie parcjalne wynosi 0,21at, to na jakiej głębokości ciśnienie parcjalne będzie wynosić 1,6at.
1at = 0,21at
x = 1,6at
x =1at*1,6at/0,21at=7,6at
a takie ciśnienie panuje na głębokości 66m.
Zadanie 3
Do jakiej głębokości można nurkować na czystym tlenie przy założeniu, że dopuszczalne ciśnienie parcjalne tlenu przy którym nie jest toksyczny wynosi 1.6at.?
Przy oddychaniu 100% tlenem, jego ciśnienie parcjalne jest równe ciśnieniu otoczenia (występuje tylko jeden gaz). Dopuszczamy więc nurkowanie do 6m przy użyciu czystego tlenu (ciśnienie otoczenia: 1,6 at).
Zadanie 4
Do jakiej głębokości można nurkować na nitroksie EAN 40 przy założeniu, że dopuszczalne ciśnienie parcjalne tlenu przy którym tlen nie jest toksyczny wynosi 1.6at.?
Należy ułożyć proporcję, która odpowie na pytanie, przy jakiej głębokości zostanie przekroczone ciśnienie parcjalne tlenu 1,6at. Na powierzchni (1at) ciśnienie parcjalne tlenu dla nitroksu EAN 40 wynosi 0,40at, to na jakiej głębokości ciśnienie parcjalne będzie wynosić 1,6at.
1at = 0,40at
x = 1,6at
x =1at * 1,6at/0,40at = 4at
a takie ciśnienie panuje na głębokości 30m.
Zadanie 5
Nurkując na Nitroxie EAN 40 nasycamy się azotem w stopniu mniejszym niż przy nurkowaniu na powietrzu. Wylicz ciśnienie parcjalne azotu przy nurkowaniu na EAN 40 dla głębokości 30m oraz przy jakiej głębokości występuje takie samo ciśnienie parcjalne azotu nurkując na powietrzu.
Nitrox EAN 40 posiada skład 40% tlenu i 60% azotu ciśnienie parcjalne azotu na 30m (4at) wynosi 4at x 0,60 = 2,4at powietrze posiada skład 21% tlenu i 79% azotu (wliczamy tu również inne gazy). Do obliczeń skorzystamy układając proporcję Posiadamy następujące dane: Na powierzchni panuje ciśnienie p1=1at, a ciśnienie parcjalne azotu wynosi 0,78at to przy jakim ciśnieniu p2 panuje ciśnienie parcjalne azotu 2,4at
1at -------0,78at
x--------2,40at
x = 2,4at x 1at / 0,79at
x = 3,04at
a takie ciśnienie panuje na głębokości 20,4m,
Zadanie to przedstawia jaka jest różnica w nasycaniu się azotem (czyli w dekompresji) zależnie od mieszanki, przy nurkowaniu na Nirtoksie EAN 40 i powietrzu. Nurkowanie na 30m przy użyciu Nitroksu EAN 40 odpowiada nurkowaniu na powietrzu do 20,4m.
Zobacz jaka jest różnica w dekompresji, przy korzystaniu z tabel PADI RDP, lub tabel CMAS Bullmahn
Zobacz również jak obliczyć równoważną głębokość powietrzną wzór stosowany jest przez nurków nitroksowych.